肥満は、健康を損なう可能性のある過剰な脂肪沈着によって定義される慢性複合疾患である。流行病に分類され、2022年には成人の43%が過体重、そのうち30%が肥満と報告されている。
肥満とそれに関連するメタボリックシンドロームは、2型糖尿病(T2D)、心血管疾患、特定の癌、肝疾患、胃腸障害、精神疾患など、驚くほど広範囲に及ぶ危険因子である。近年では、アルツハイマー病(AD)、パーキンソン病(PD)、多発性硬化症(MS)、筋萎縮性側索硬化症(ALS)など、いくつかの神経変性疾患の重要な危険因子として認識されるようになった。
食事脂肪の過剰摂取を特徴とする高脂肪食は、肥満の一因であることがよく知られている。動物実験では、肥満を誘発し、代謝に及ぼす影響を研究するために、高脂肪食が頻繁に用いられている。ストレプトゾトシンは、膵島のβ細胞に選択的に毒性を示す天然由来の化合物であり、動物モデルにおいてT2Dを誘導するために一般的に用いられている。T2Dは、インスリン分泌の異常と循環インスリンの機能的効率の低下によって特徴づけられる。
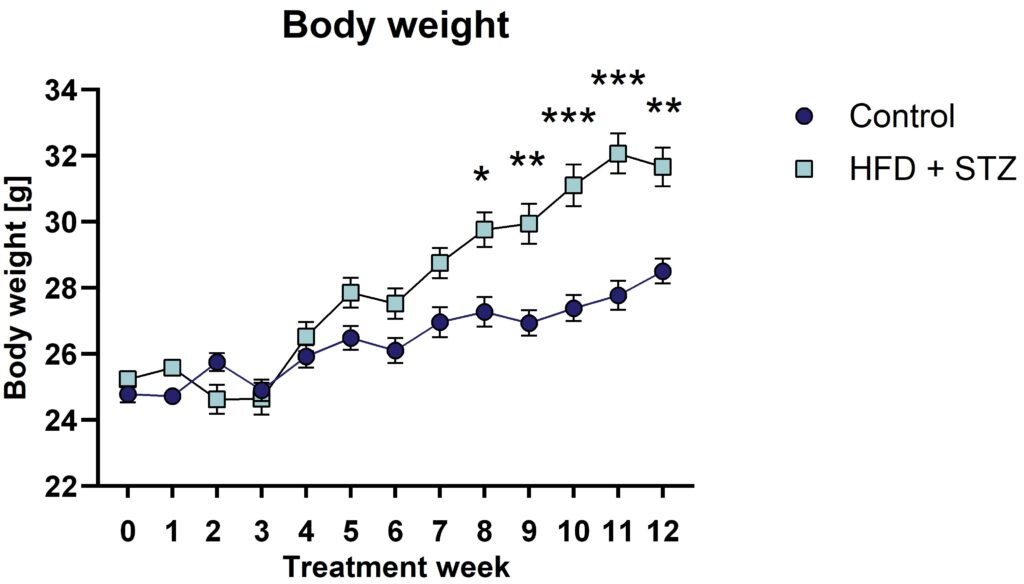
図1:T2D誘発マウスの経時的体重増加。 高脂肪食(HFD)とストレプトゾトシン(STZ)を投与した動物は4週目以降体重が増加し始め、8週目には対照動物と比較して体重が有意に増加した。0週目=ベースライン。平均値+SEM;二元配置分散分析(way-way ANOVA)後、Bonferroniのpost hoc検定、n=16-19の雌雄混合動物/群、時点。
Scantox トランスジェニック動物および非トランスジェニック動物において、糖尿病の併発の有無にかかわらず、肥満モデルを提供する。動物は体重増加(図1)と摂餌量の増加、グルコース値(図2A)とコレステロール値(図2B)の上昇を示す。モデルによっては、肝機能障害や他の代謝変化と同様に、軽度の認知障害も起こりうる。さらに、APPSL x hQCトランスジェニック動物でT2D糖尿病をモデル化すると、不溶性の38-、40-および42-アミロイドβのレベルが上昇する(詳細については、論文Adekunle Babalolaら、2024を参照)。
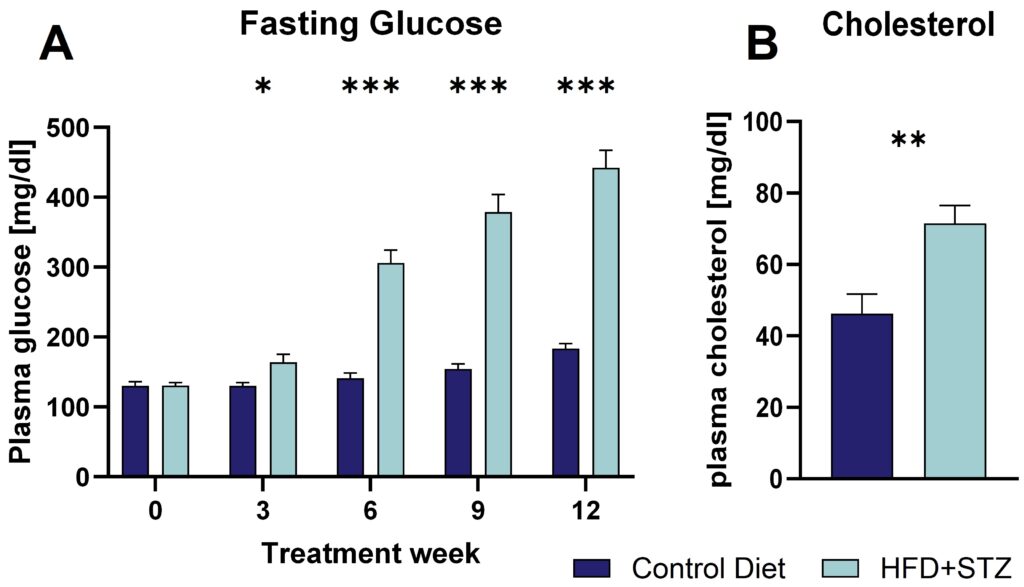
図2:T2Dを誘発した動物における空腹時血糖値とコレステロール値の変化。 血糖パラメーターの変化(A)は、T2D誘導後3週目にすでに観察された。平均値+SEM;二元配置分散分析(way-way ANOVA)後、Bonferroniのポストホック検定;n=16-19の雌雄混合動物/群・時点。T2D誘導14週後の血漿コレステロール値の変化(B)。0週目=ベースライン。平均値+SEM;両側t検定、各群n=7-8雌雄混合動物。*p<0.05; **p<0.01; ***p<0.001。HFD:高脂肪食,STZ:ストレプトゾトシン,T2D:2型糖尿病。
Scantox は、T2Dモデルのためのカスタムメイドの試験デザインを提供し、あなたの特別な関心に柔軟に対応します。また、研究デザインに関するアドバイスやご提案もさせていただきます。T2Dモデルは誘導モデルであるため、驚くほど短い納期が可能です。Scantox 、トランスジェニックマウスモデルのコロニーを所有しています。
これらのマウスモデルで貴社の化合物を試験させていただければ幸いです!読み出し値はモデルによって異なりますが、最も一般的なものは以下の通りです:
- 体重
- 食品消費とカロリー摂取
- 学習・記憶障害
- 血糖パラメーター(空腹時インスリンとグルコース、HOMA-IR、HOMA-β)
- 耐糖能とインスリン感受性
- 全腸移行時間と胃排出障害
- 脂肪組織の採取と重量(例:mWAT、eWAT)
- コレステロール値(総コレステロール値、遊離コレステロール値、エステル化コレステロール値)、HDL値、LDL値、トリグリセリド値
- コレステロール代謝関連遺伝子発現(q RT-PCR)
- 血漿中のアスパラギン酸アミノトランスフェラーゼ(AST)、アラニンアミノトランスフェラーゼ(ALT)、アルカリホスファターゼ(ALP)値
- 炎症マーカー
- BBB機能不全/漏出
ご興味のある方はこちらもご覧ください:
お問い合わせをお待ちしております。
