多発性硬化症(MS)はヒト特有の疾患であり、若年成人に最も多くみられる神経疾患の一つである。
神経症状は多岐にわたり、病気の進行も様々であるが、主な特徴は、脱髄、神経炎症、神経変性であり、その結果、持続的な障害が生じる。
MSのモデル化と新薬の試験には、実験的自己免疫性脳脊髄炎(EAE)モデルがよく用いられる。
ここでは、10週齢の雌性C57Bl/6マウスにMOGと百日咳毒素を投与してEAEを誘発し、頚髄における神経炎症と脱髄を評価した。
EAEを誘発した1群には、病態を予防するために参考項目としてフィンゴリモドを慢性的に投与した。
CD45(図1、代表画像)およびIba1レベル(図1)の上昇によって示されるように、EAE誘発は頸髄に強い炎症を引き起こすことがわかる。
フィンゴリモドによる治療は、このモデルの神経病理学的特徴を軽減することができ、したがって貴重な陽性対照となる。
同じ動物で髄鞘形成を評価したところ、EAE誘発マウスでは偽薬投与マウスに比べて髄鞘が強く減少していた(図2)。
さらに、血漿中のニューロフィラメント-軽鎖(NF-L)レベルを解析したところ、EAE誘発によってレベルが非常に上昇したが、フィンゴリモド治療によって防ぐことができた(図2)。 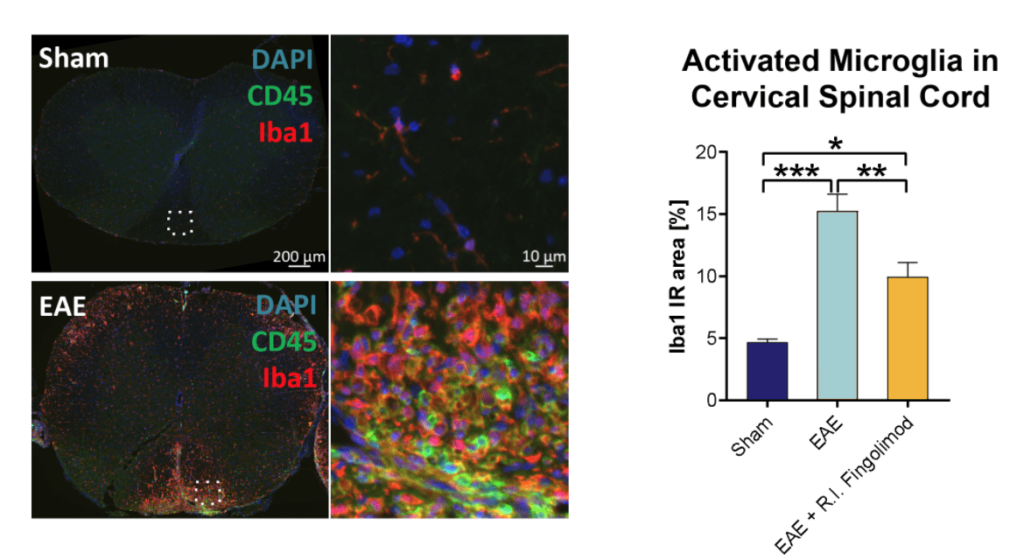
図1. 頚髄における神経炎症。 CD45標識による白血球、Iba1標識による活性化ミクログリア、DAPIによる核のカウンターステインを示す免疫蛍光標識の代表画像(偽薬投与マウスとEAE誘発マウス)。
グラフは、偽薬投与マウス、EAE誘発マウス、およびフィンゴリモドを追加投与したEAE誘発マウスの頚髄白質におけるIba1の免疫反応面積(%)を示す。
グラフは、マウス1匹につき1-2脊髄切片の関心領域内で測定した免疫蛍光シグナルの平均値を示す(各群n = 6-8)。
一元配置分散分析の後、Bonferroniのポストホック検定を行った。
平均値+SEM。
*p<0.05; **p<0.01; ***p<0.001。
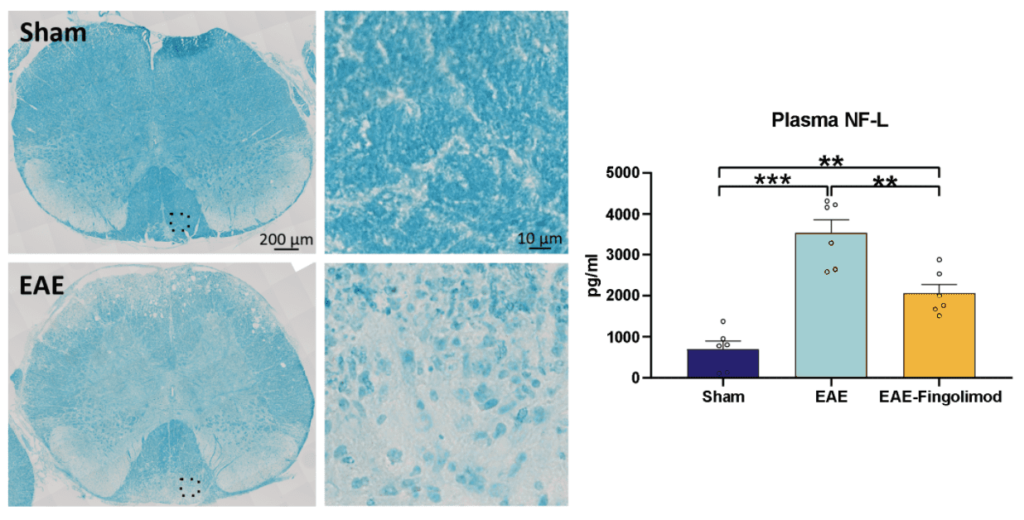
図2. EAEマウスモデルにおける神経変性過程。 偽薬投与マウスとEAE誘発マウスのミエリンを示すLuxol Fast Blue染色の代表画像。
EAE誘発マウスでは染色が弱く、脱髄を示している(左)。
偽薬投与マウス、EAE誘発マウス、フィンゴリモドを追加投与したEAE誘発マウスの血漿中のニューロフィラメント-軽鎖レベルの定量。
(各群n = 6)。
一元配置分散分析(One-way ANOVA)とTukeyのポストホック検定。
平均値+SEM。
**p<0.01; ***p<0.001。EAE誘発マウスモデルでの試験をご希望の方は、今すぐお問い合わせください!








