前頭側頭型認知症(FTD)、進行性核上性麻痺(PSP)、皮質基底核変性症(CBD)はすべて、脳の重要な構造タンパク質であるタウの異常という共通点を持つ神経変性疾患である。
現在、カリフォルニア大学サンタバーバラ校の研究者たちは、ミスフォールディングしたタウ蛋白質からなる神経原線維のもつれの形成を阻害する方法を発見した可能性がある。
この研究はまだ初期段階だが、神経変性を標的とした画期的な治療介入への道を開く可能性がある。
タウタンパク質が脳機能を阻害するメカニズム
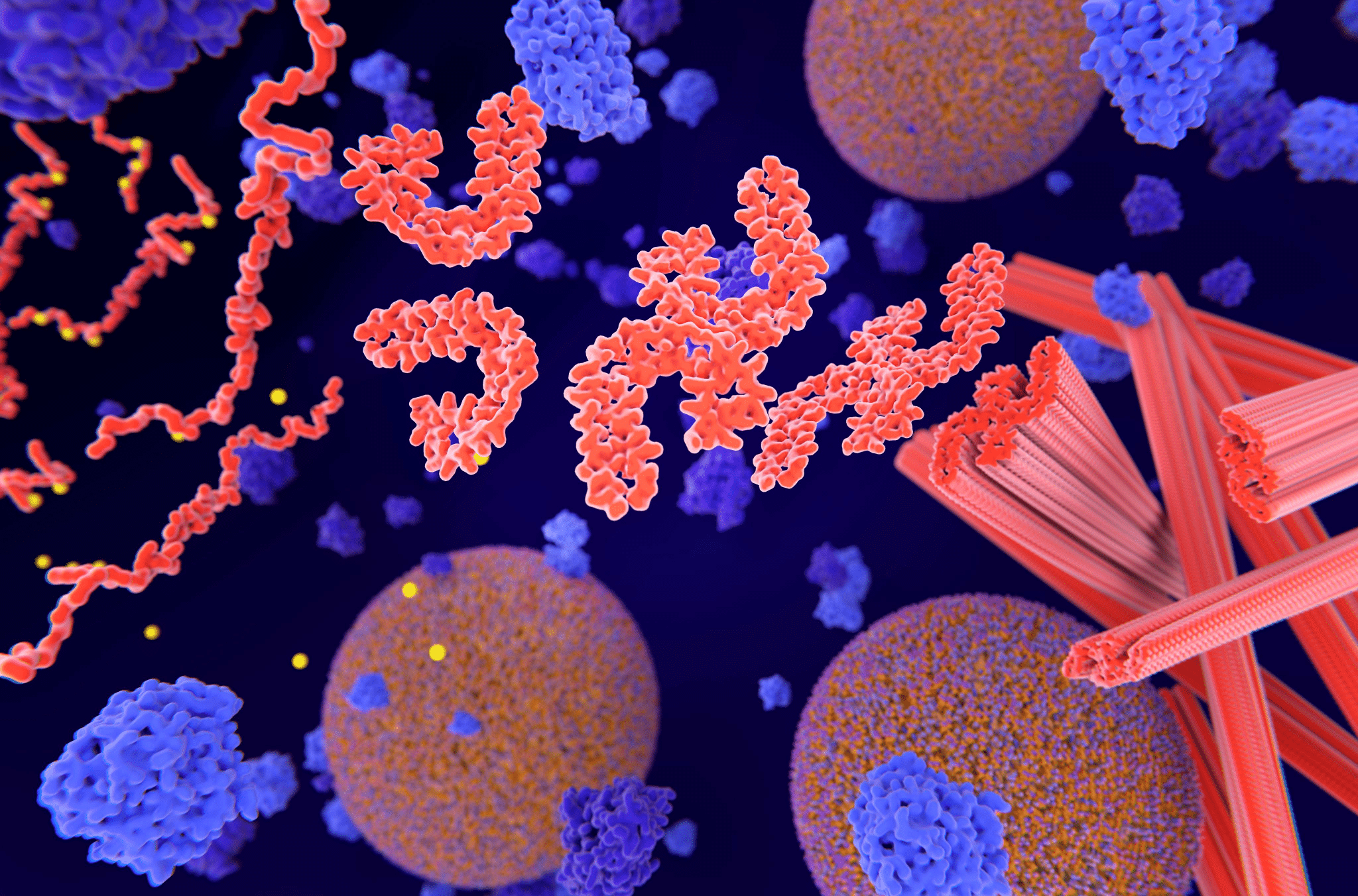
タウ蛋白質は脳の健康に重要な役割を果たしており、安定した細胞の形成と構造の維持を助けると同時に、脳内の栄養輸送を促進している。
残念なことに、異常なタウ、具体的にはミスフォールディングを起こし、その構造を損傷し、粘着性のあるもつれた表面を形成したタウは、神経原線維のもつれを形成することにより、多くの神経変性疾患の一因となっている。
個々のミスフォールディングしたタウ蛋白質は、しばしばドミノ効果を起こし、正常なタウ蛋白質にもミスフォールディングを引き起こし、機能不全蛋白質の蓄積を引き起こす。
この蓄積は、時間の経過とともに脳機能を阻害し、タウオパチーと呼ばれる壊滅的な神経変性障害を引き起こす可能性がある。
このことを念頭に置いて、カリフォルニア大学サンタバーバラ校の研究チームは、「もし、タウのミスフォールディングを未然に防ぐことができたらどうだろうか?
タウタンパク質の異常を理解する
一般に神経変性疾患には、短い「3回繰り返し」(3R)型と長い「4回繰り返し」(4R)型の2種類のタウが関連している。
FTD、PSP、CBDのような疾患は、特に4Rタウの蓄積を伴う。
4Rタウがどのようにしてミスフォールドし始めるのかを理解するため、カリフォルニア大学サンタバーバラ校の研究者たちは、細胞培養実験と透過型電子顕微鏡や分子動力学シミュレーションなどの高度な技術を組み合わせた。
入念な研究により、研究チームは4Rタウに存在するユニークな「ヘアピン」構造を特定することができた。
その構造の中に、PHF6と呼ばれる粘着性のセグメントを発見した。PHF6は、他のタウタンパク質と結合し、より大きな構造へと積み重ねることができるため、ミスフォールディングの可能性があるタンパク質の蓄積を促進するという意味で粘着性がある。
研究チームは、PHF6を阻害することで、タウタンパク質が広範囲に形成され蓄積される可能性を減らすことができるのではないかと考えた。
PHF6を標的とする
最後に、今後の研究の道筋をつけるために、PHF6に結合できる物質を特定する必要があった。
研究チームは、リャマなどラクダ科の動物の血液から合成されたナノボディ(抗体の小さな断片)に注目した。
ラクダ科のナノボディは現在、治療的介入がPHF6領域に結合し、タウの凝集を抑制するのを助ける潜在的な手段と考えられている。
研究チームは今後、ラクダ科動物のナノボディーを精査し、ナノボディーをPHF6に結合させる正確な因子を特定することを目指す。
カリフォルニア大学サンタバーバラ校の研究チームは、まだ初期段階にあるが、治療的介入を推進するための2つの重要な要因を特定した。第1に、標的とする正確な4R領域、第2に、介入を標的に結合させる可能性のあるビークル(ナノボディ)である。
研究チームは、神経原線維のもつれ形成を抑制する有効な治療法を特定するまでには、まだ長い道のりがある。
将来的には、動物モデルを用いてこの技術をテストし、タウの凝集を解きほぐす方法、あるいは凝集を完全に防ぐ方法について、より理解を深めることが理想である。
継続的な研究により、科学界は制御不能なタンパク質を除去し、神経変性疾患を持つ無数の人々の治療と生活の質を改善することに一歩近づくことができるだろう。Scantoxは、1977年以来、最高グレードの薬理学および規制毒性学サービスを提供する、北欧を代表する前臨床GLP認定CRO(医薬品開発業務受託機関)である。
SCANTOXは前臨床試験受託サービスに重点を置き、製薬企業やバイオテクノロジー企業の医薬品開発プロジェクトをサポートしています。
コアコンピテンシーには、探索的試験、有効性試験、PK試験、一般毒性試験、局所耐性試験、創傷治癒試験、ワクチンなどがあります。
SCANTOXの詳細については、https://scantox.com。