神経変性疾患や希少疾患の研究分野において、ウイルス注射はますます不可欠なものとなりつつある。 この方法では、海馬、大脳皮質、線条体、脳室、その他ほとんどすべての脳領域への定位注射、あるいは標的タンパク質のcDNAやshRNAを発現するウイルス粒子の静脈内注射によって、標的タンパク質を明確な脳領域で発現または抑制することができる。
ScantoxのAAALAC認定動物施設は、レンチ、アデノおよびアデノ随伴(AAV)ウイルス粒子注射などを含むがこれに限定されない、マウスおよびラット実験のためのバイオセーフティレベル2(BSL2)実験室を維持している。
この方法は、アルツハイマー病、パーキンソン病、タウオパチー、筋萎縮性側索硬化症、いくつかのライソゾーム貯蔵病、自閉症スペクトラム障害など、さまざまな疾患に特異的なタンパク質をマウスやラットで誘導したり抑制したりするのに用いることができる。 したがって、この方法は遺伝子治療のアプローチにも大いに関連する。
SCANTOXでよく使われるウイルス誘発げっ歯類モデルは以下の通りである:
- AAV2 hA53T α-シヌクレイン誘発パーキンソン病
- AAV9 TDP-43誘発筋萎縮性側索硬化症
- AAV9タウP301L誘導タウ播種(下記参照)
タウ・シーディング
アルツハイマー病やその他の認知疾患の誘発や治療に対する特定のウイルスの効果を分析するために、マウスの内嗅皮質(ERC)への注射を行うことができる。
今回発表した播種研究では、AAV9 Tau P301LをAPPSLマウスのERCに注射し、注射1ヵ月後に海馬におけるタウの拡散を観察した(図1)。
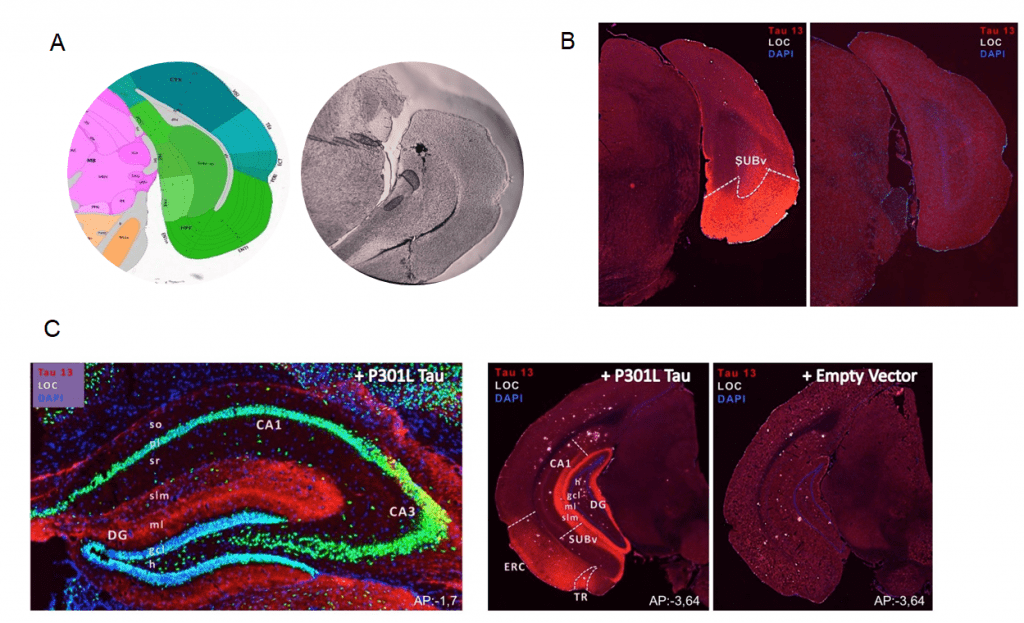
図1:ヒトタウP301L遺伝子を組み込んだ血清型9の組換えアデノ随伴ウイルス粒子(AAV9)または空のベクターを3ヶ月齢の雄APPSLマウスのERCに脳内注射した。A:ERCへのインク注入による注入部位の確認。B:AAV9タウP301Lウイルス注入後のERCにおけるタウ発現。C: APPSLマウスのERCへのAAV9 Tau P301L注射後の海馬へのタウの広がり。 すべての解析はウイルス注入1ヶ月後に行った。
ウイルス注射によるタンパク質の誘導は、ほとんどの神経変性疾患やライソゾーム貯蔵疾患のモデルに適用できる汎用性の高い方法であり、一方、タンパク質の抑制は、生体内での タンパク質の機能や遺伝子治療アプローチの有効性を評価するのに有用である。あなたの研究分野へのこの方法の適用可能性について、今すぐご相談ください。
SCANTOXでは、ウイルス誘発げっ歯類モデルについて、お客様のご希望に沿った試験デザインをご提案しております。 また、研究デザインに関するアドバイスやご提案もさせていただきます。 ウイルス誘発モデルは、多くの場合、治療後すぐに関連する疾患表現型を示します。 そのため、研究期間を大幅に短縮することができます。 さらに、適切な試験デザインに必要なコントロールとして、偽/ビヒクル処置マウスを使用することができます。
弊社では、ウイルス誘発げっ歯類モデルで貴社の化合物の有効性を評価することを喜んでお引き受けいたします! 最も一般的な測定値はモデルによって異なり、以下のようなものがあります:
以下の関連トピックにもご興味があるかもしれません:
