B6.SOD1G93Aトランスジェニックマウスは、コンジェニックC57BL/6バックグラウンドで育種され、一般的に使用されているSOD1(*G93A)1Gurマウスに代わる説得力のあるマウスである。
このマウスは、従来C57BL/6xSJLの混血で飼育されていたオリジナル系統と比較して、筋萎縮性側索硬化症(ALS)特異的表現型の進行がわずかに遅い。
ALSの病勢が緩徐であるため、治療的介入の可能性が広がり、新たな治療戦略につながる可能性がある。
B6.SOD1G93Aマウスの筋電図(EMG)評価では、ntg同腹子と比較して、複合筋活動電位(CMAP;図1A)と運動単位活動電位(MUAP;図1B)が持続的に低下していることが明らかになった。
筋電図観察と一致して、B6.SOD1G93Aマウスは、握力試験(図1C)およびワイヤー掛け試験(図1D)の成績低下で明らかなように、筋力の進行性低下を示した。 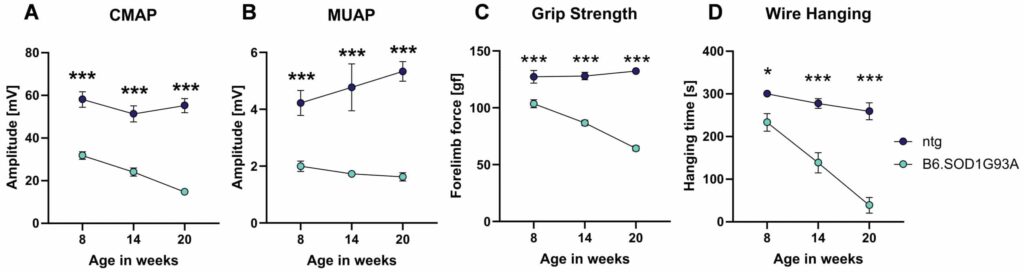
図1:縦方向の筋電図記録と筋力分析。 CMAPによる筋電図記録
(A)とMUAP
(B)の測定。
握力テストにおける前肢最大筋力の分析による筋力測定。
(C)およびワイヤーハンギングテストにおけるハンギングタイム
(D).
すべての解析は、B6.SOD1G93Aマウスをntg同腹子と比較し、8週齢、14週齢、20週齢で行った。
遺伝子型を主因子とした二元配置分散分析、Bonferroniのポストホック検定。
平均値±SEM。
*p<0.05; ***p<0.001。
n=16/群。
さらに、B6.SOD1G93Aマウスは、血漿中ニューロフィラメント軽鎖(NF-L)レベルの上昇(図2A)によって示されるように、14週齢で明らかな神経変性を示し、時間の経過とともに徐々に悪化し、20週齢で顕著な神経変性に至った。
さらに、オートファジーマーカーp62レベルは、脊髄の頸部、胸部、腰部において20週齢で増加している。 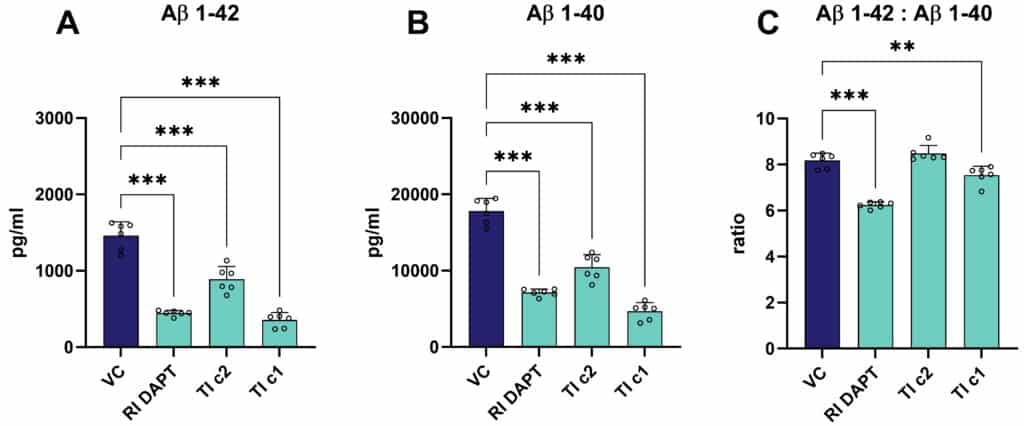
図2:B6SJL.SOD1-G93Aマウスにおける神経細胞の消失とオートファジー。 A:8週齢、14週齢、20週齢のB6.SOD1G93Aマウスの血漿中NF-Lの定量をntg同腹子と比較。
B:20週齢のB6.SOD1G93Aマウスとntg同腹子の頚髄、胸髄、腰髄におけるオートファジーマーカーp62の定量を曲線下面積(AUC)で評価。
A-D:二元配置分散分析(Two-way ANOVA)とBonferronipost hoctest。
平均値+SEM。
n=4-8/群。
*p<0.05; **p<0.01 ***p<0.001。
B6.SOD1G93Aマウスで観察された進行性の運動障害と神経変性は、ヒトのALSの表現型を再現しており、このマウスはALSの病態メカニズムの根底にあるものを調べるための貴重なモデルである。
観察された進行の遅さは、薬理学的介入に有利なウインドウの延長をもたらす。
行動学的評価に加え、反復筋電図評価やin vivo血漿サンプルのNF-L分析などの縦断的指標を追加することで、ALSと闘うことを目的とした薬剤候補をより微妙で高感度に評価することが可能になる。
B6.SOD1G93Aマウスを用いたin vivo試験の開始については、今すぐお問い合わせください。








