ポンペ病モデルマウスとして若い6neoマウスの筋力低下と運動障害を検証した後、我々の研究チームは、このライソゾーム貯蔵病モデルマウスの非神経細胞組織と神経細胞組織における酵素の減少とグリコーゲン基質レベルを検証するために、酸性α-グルコシダーゼ(GAA)酵素活性を評価した。
そこで、ポンペ6neoマウスの大腿四頭筋と皮質組織を、それぞれ4-MUGベースのGAAアッセイと市販のグリコーゲンアッセイキット(Sigma, MAK016-1KT)を用いて、GAAとグリコーゲンレベルについて分析した。
24週齢の6neoマウスでは、大腿四頭筋と大脳皮質でGAA活性が高度に低下しており(それぞれ図1AとB)、ポンペ病治療薬開発におけるこのモデルマウスの価値が検証された。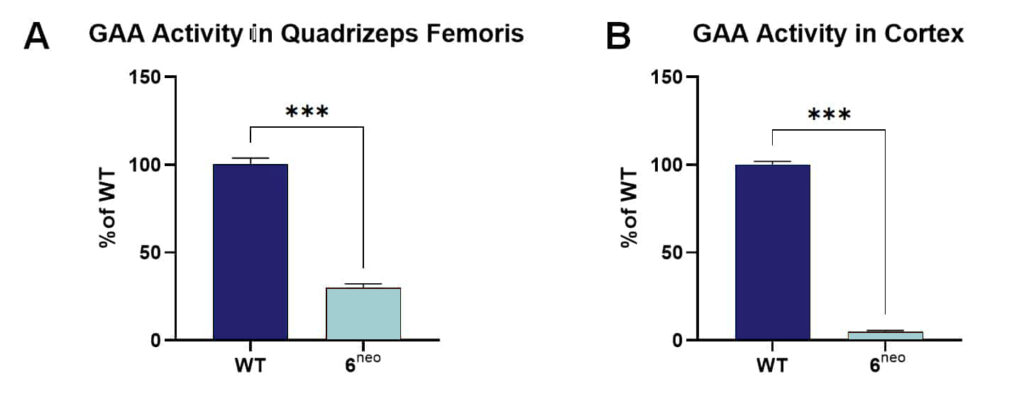 図1:6neoマウスの大腿四頭筋および大脳皮質におけるα-グルコシダーゼ(GAA)活性。大腿四頭筋
図1:6neoマウスの大腿四頭筋および大脳皮質におけるα-グルコシダーゼ(GAA)活性。大腿四頭筋
(A)と皮質組織
(24週齢の6neoマウスの大腿四頭筋(A)と皮質組織(B)のGAA活性を解析した。
n = 16/群;平均値+SEM;不対t-検定;***p<0.001。
6neoマウスの大腿四頭筋では、4週齢ですでにグリコーゲンレベルが非常に上昇している。
年齢とともに、グリコーゲンレベルはさらに上昇する(図2A)。
大脳皮質のグリコーゲンレベルを評価したところ、4週齢では有意な変化は見られなかったが、24週齢でグリコーゲンレベルが非常に上昇し、加齢とともにさらに増幅した(図2B)。
このように、基質の蓄積は非神経細胞組織ではより早く始まる。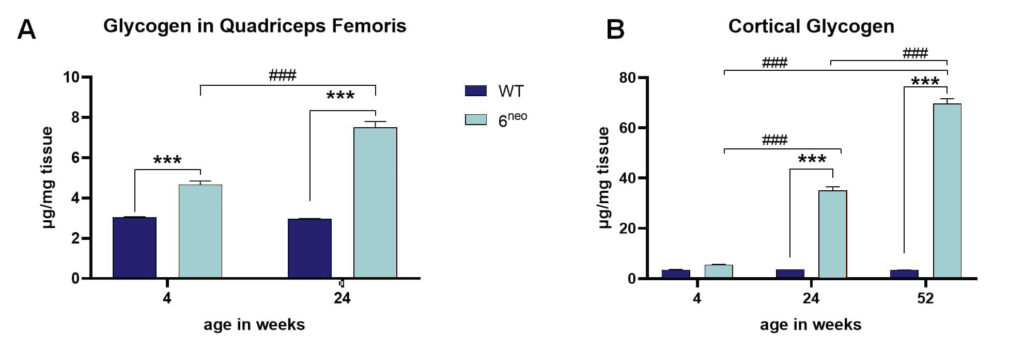 図2:6neoマウスの大腿四頭筋および大脳皮質におけるグリコーゲンレベル。4週齢と24週齢の6neoマウスの大腿四頭筋(A)と、4週齢、24週齢、52週齢の6neoマウスの皮質組織(B)のグリコーゲン量を分析した。 n = 16/群;平均値+SEM;二元配置分散分析(ANOVA)後、ボンフェローニの多重比較ポストホック検定;***/###p<0.001;*遺伝子型間の有意性;#年齢群間の有意性。
図2:6neoマウスの大腿四頭筋および大脳皮質におけるグリコーゲンレベル。4週齢と24週齢の6neoマウスの大腿四頭筋(A)と、4週齢、24週齢、52週齢の6neoマウスの皮質組織(B)のグリコーゲン量を分析した。 n = 16/群;平均値+SEM;二元配置分散分析(ANOVA)後、ボンフェローニの多重比較ポストホック検定;***/###p<0.001;*遺伝子型間の有意性;#年齢群間の有意性。
我々は以前、8週齢で初めてin vivoでの筋欠損を観察したように、グリコーゲン基質の蓄積はin vivoでの変化を進行させるようである。
これらの結果は、6neomiceがポンペ病を研究し、この病気の壊滅的な症状を改善するために有効な新規化合物を試験するための貴重なツールであることをさらにアピールするものである。6neo マウスを用いた研究をご希望の方は、今すぐ弊社までご連絡ください!
科学ニュース
脳内ロテノン投与によるパーキンソン病発症機序の解明
May 26, 2025
細胞からマウスへ:ゴーシェ病研究のための患者由来モデルと前臨床モデル
April 23, 2025
すべては加齢のせい
March 26, 2025
ブログ

初期アルツハイマー病発症の窓としての血漿GFAP:5xFADマウスモデルからの機序的洞察
July 9, 2025

ニーマン・ピックC型における治療法の拡大:新規BMPヒドロラーゼ標的としてのPLA2G15
July 2, 2025

脳細胞プラットフォームが画期的なアルツハイマー治療薬ALT001につながる
June 24, 2025

神経経路オルガノイドが痛みのシグナルに迫る
June 17, 2025
会社ニュース

Scantox AAALACの完全認定を取得-動物福祉と科学的誠実さへの取り組みを強化
June 27, 2025

アニュアルレポート2024を発表
April 28, 2025

ACT 2024:Scantox 「拡大するトキシコロジー・サービス」で一歩先を行く
November 4, 2024

Scantox、ESGCT 2024で細胞・遺伝子治療能力を披露
September 29, 2024

