GCase活性の低下は、ゴーシェ病の主要な特徴である。
乾燥血液スポット(DBS)として採取した少量の全血から、複数の時点におけるGCase活性の変化をモニターすることにより、薬効に関する貴重な新しい知見を得ることができる。
ヒトグルコシルセラミダーゼβ(GBA)遺伝子の変異とそれに伴うGCase活性は、ゴーシェ病(GD)の原因である。
ゴーシェ病におけるグルコシルセラミダーゼβ(GBA)遺伝子の変異とそれに伴うGCase活性は、ゴーシェ病の原因遺伝子である。
薬剤候補のスクリーニングや、前臨床モデルにおける酵素置換療法や遺伝子治療アプローチの試験のためのトランスレーショナルリードアウトは常に開発され、改良されている。
GCase活性の評価を含むDBS分析は、患者におけるGDの診断とモニタリングのためのゴールドスタンダードとなっている。
DBSは、必要な全血量が最小限であること、保存が容易であること、持ち運びが可能であることなどから、臨床応用に実用的なソリューションを提供する。
同じ利点が動物実験にも当てはまります。しかし、さらに少量の血液を扱う場合には課題が生じ、一貫した再現性のある結果を得ることが難しくなります。
SCANTOXでは、最小限の全血を用い、DBSサンプルを用いた4-MUGベースのGCase活性測定法を最適化しました。
このアプローチにより、マウスの複数のin vivoサンプリングから得られた血液を利用し、GCase活性を漸進的にモニターすることが可能となり、単一のエンドポイント測定に依存することがなくなりました。
以下のデータは、脳内で評価されたGCase活性の比較分析である。
(A)とDBSサンプル
(B) 4ヶ月齢のGBA D409V KIマウスに由来し、これらの測定値が一致することを強調している。
ホモ接合体(tm/tm)、ヘテロ接合体(tm/wt)、野生型(wt/wt)の同腹子の脳とDBSサンプルを分析したところ、どちらのサンプルタイプでも遺伝子投与量に依存したGCase活性の低下が明らかになった(図1参照)。 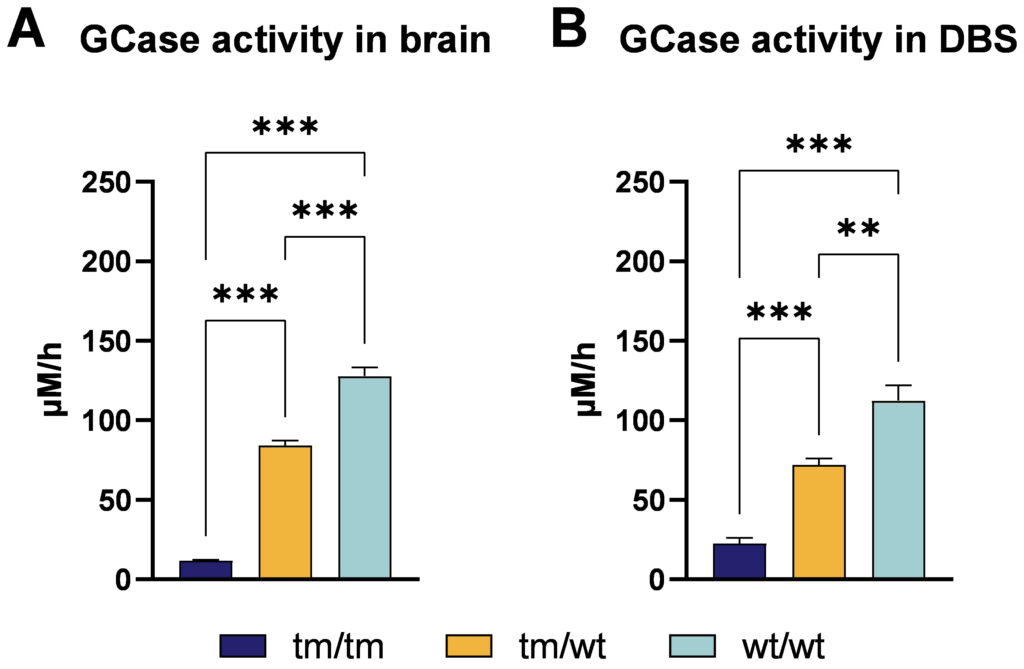
図1:GBAD409V KIマウスの脳とDBSにおけるGCase活性。 4ヶ月齢のホモ接合体(tm/tm)、ヘテロ接合体(tm/wt)、野生型(wt/wt)の同腹子の脳とDBSサンプルを、4-MUGベースのアッセイを用いて分析した。
一元配置分散分析、Bonferroniの多重比較ポストホック 検定;平均値+SEM;各群n = 6;**p<0.01、***p<0.001。
tm、標的変異。ゴーシェ病研究の開始については、今すぐお問い合わせください!