타우 단백질은 미세소관 관련 단백질 계열에 속하며 신경세포 미세소관 네트워크를 안정화시키는 데 중요한 역할을 합니다. 타우 단백질은 알츠하이머병과 진행성 핵상 마비(PSP), 피질 기저부 변성(CBD), 픽병(PiD), 무수축성 곡물병, 염색체 17(FTDP-17)과 관련된 유전성 전측두엽 치매 및 파킨슨병 등 ‘타우 병증’으로 불리는 수많은 신경 퇴행성 장애의 주요 구성 성분입니다.
분자 분석을 통해 타우의 과인산화가 신경 퇴행과 치매를 유발하는 타우 응집으로 이어지는 중요한 사건일 수 있다는 사실이 밝혀졌습니다. 타우 과인산화를 방지할 수 있는 새로운 화합물의 개발은 점점 더 뜨거운 화두가 되고 있습니다.
따라서 인간 질환에서 타우 과인산화를 반영하는 신뢰할 수 있는 모델이 필요합니다. 이를 위해 두 가지 질병 관련 돌연변이(V337M/R406W)를 포함하는 가장 긴 인간 타우441 동형체를 과발현하는 SH-SY5Y 세포주를 안정적으로 감염시켜 생성했습니다. SH-SY5Y-TMHT441 세포에서 타우의 인산화 패턴은 여러 키나아제 억제제에 의해 안정적으로 조절될 수 있습니다. 타우 인산화에 대한 영향(예: Thr181, Ser202, Thr231/Ser235, Ser262 및 Ser396/Ser4049)은 면역 흡착 분석(MSD), 면역 블롯 분석 또는 질량 분석법을 포함한 다양한 방법으로 확인할 수 있습니다(Löffler T. et al, J Mol Neurosci 2012 May;47(1):192-203).

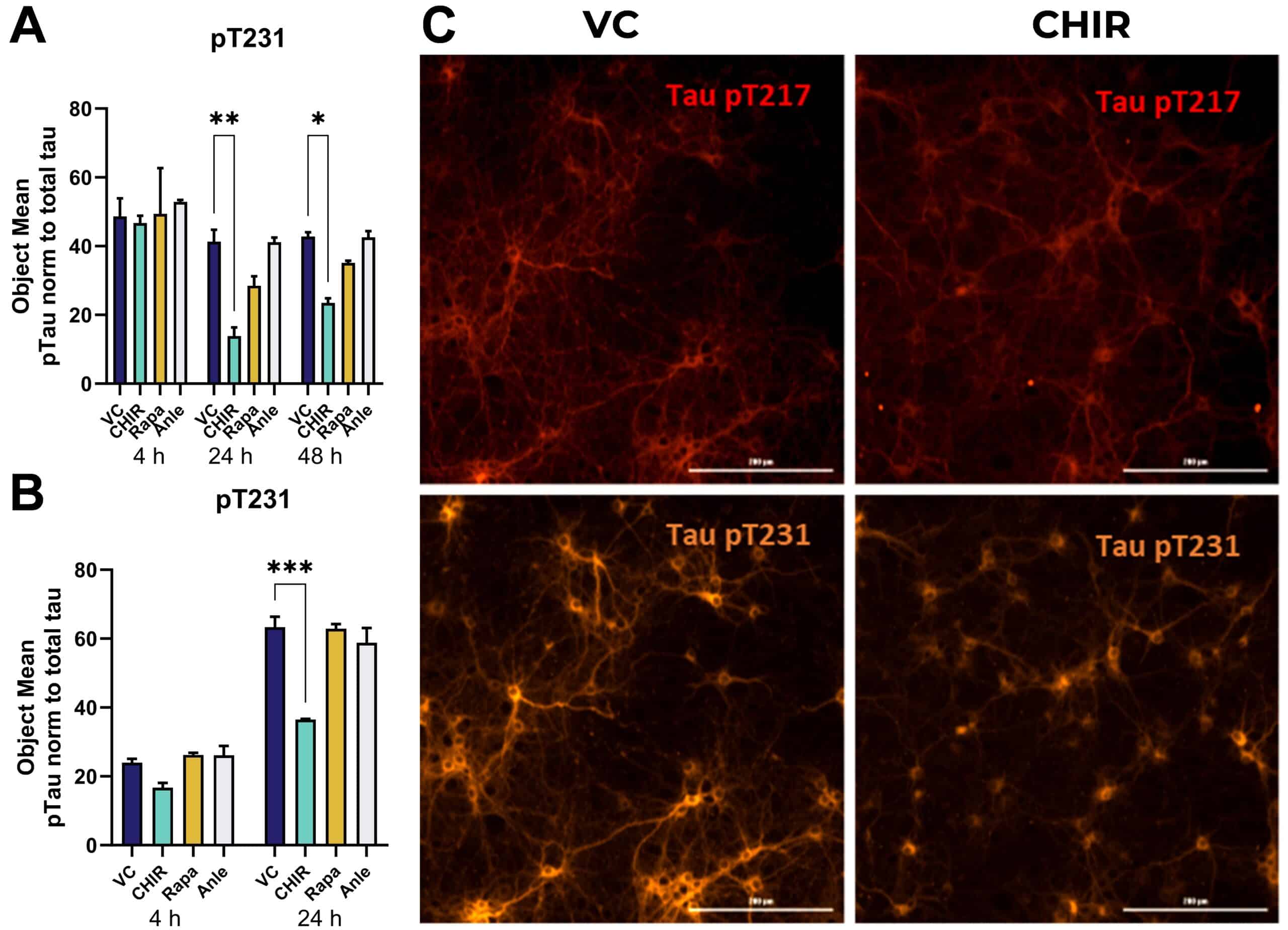
그림 1: 화합물로 8시간 및 24시간 배양한 후 V337M/R406W 돌연변이가 있는 2N4R 타우를 과발현하는 분화 안정적으로 감염된 SH-SY5Y 세포주에서의 타우 인산화. 20mM LiCl, 1µM CHIR99021 및 1µM GSK-3β VIII로 처리한 후 8시간(A, B) 또는 24시간(C, D) 후에 채취한 세포의 RIPA 추출물을 MSD 면역 흡착 분석법으로 Ser202 및 Ser396에서 인산화된 타우를 평가했습니다. Dunnett의 다중 비교 테스트와 차량 대조군(VC)을 사용한 일원 분산 분석(One-Way ANOVA). 평균 ± SEM; n = 6. **P<0.01; ***P<0.001.
P301L 돌연변이를 보유한 가장 긴 인간 Tau441을 과발현하는 SH-SY5Y 세포 또는 PS19 마우스와 같은 형질전환 마우스의 1차 뉴런에서도 동일한 분석법을 설정할 수 있습니다.