타우병증 환자의 정제된 타우 응집체를 마우스 뇌에 주입하면 타우병증 환자의 주요 병리학적 특징을 요약할 수 있습니다.
따라서 이 접근법은 높은 번역 가치를 지닌 타우병증 특이적 병리를 분석할 수 있습니다.
주사를 위해 인간 타우를 발현하지만 내인성 타우가 없는 생후 9~10주 된 hTau 마우스를 사용했습니다.
마우스의 해마와 두정엽 피질에 AD 브락 6기 환자의 사르코실 불용성 타우 씨앗을 일방적으로 주입했습니다.
주사 12주 후 동물을 희생하고 뇌를 분석하여 세린 202/트레오닌 205(pSer202/pThr205)에서 인산화 타우의 병리학적 변화를 확인했습니다.
인산화 타우는 해마의 피질과 해마뿐만 아니라 반대쪽 반구에서도 측정할 수 있었으며, 이는 타우 시딩과 타우가 반대쪽으로 퍼지는 것을 나타냅니다(그림 1). 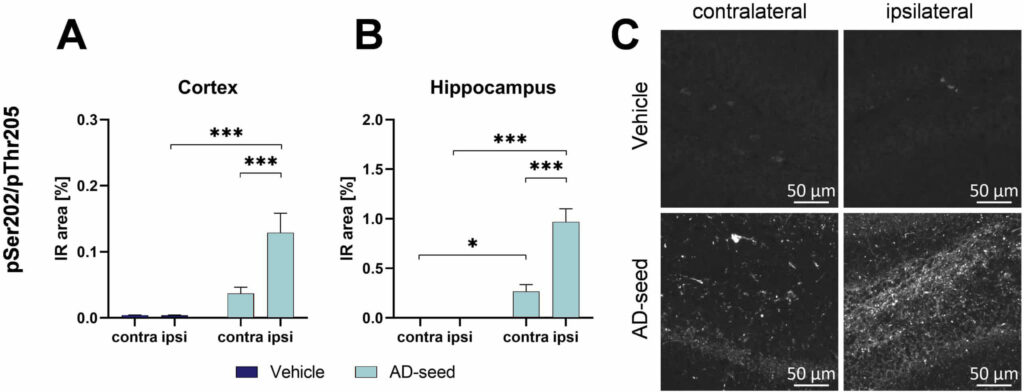 그림 1: 대측 및 동측 반구의 두정엽 피질(A) 및 해마(B, C)에서 일측 AD 뇌종자를 해마 및 동측 반구의 상피질에 주입한 후 pSer202/pThr205 타우 면역 반응성.
그림 1: 대측 및 동측 반구의 두정엽 피질(A) 및 해마(B, C)에서 일측 AD 뇌종자를 해마 및 동측 반구의 상피질에 주입한 후 pSer202/pThr205 타우 면역 반응성.
주사 12주 후 동물을 안락사시키고 AT8 항체를 사용하여 뇌를 평가했습니다.
IR = 면역 반응 영역.
n = 8 / 그룹; 이원 분산 분석(2-way ANOVA)과 다중 비교를 위한 시다크 사후 검정; 평균 + SEM.
*p<0.05; ***p<0.001.
뉴런, 성상세포증 및 세포핵 표지 마커를 사용하여 뇌 조직 절편을 면역 조직학적으로 분석한 결과, 주입된 동측 반구의 상아교 과립 세포 층의 구조적 변화가 나타났습니다(그림 2). 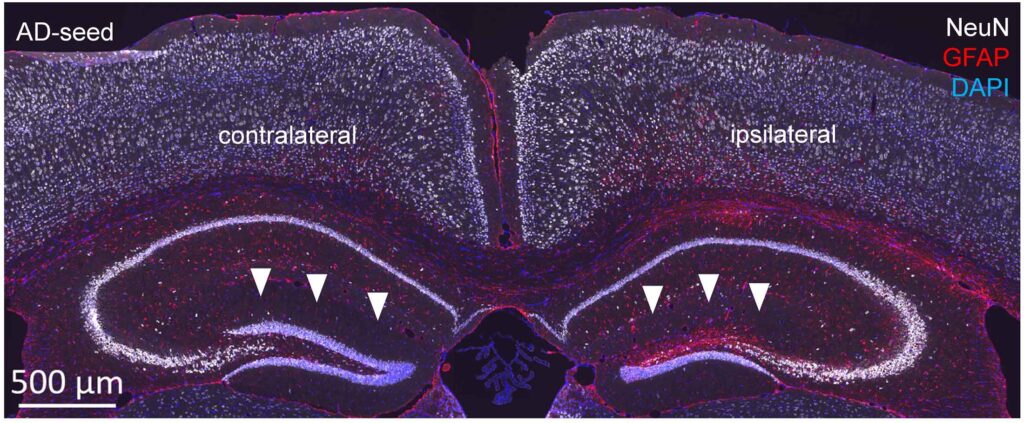 그림 2: 신경세포 체세포의 마커인 NeuN과 성상교세포증의 마커인 아교 섬유소 산성 단백질(GFAP)의 면역 형광 표지, 그리고 세포 핵을 시각화하기 위한 DAPI 염색.
그림 2: 신경세포 체세포의 마커인 NeuN과 성상교세포증의 마커인 아교 섬유소 산성 단백질(GFAP)의 면역 형광 표지, 그리고 세포 핵을 시각화하기 위한 DAPI 염색.
타우 종자를 주입한 동측과 반대쪽 대조군 사이의 상아교 과립 세포 층의 구조적 변화에 주목하세요(흰색 화살표 머리).
우리의 연구 결과는 알츠하이머 환자 유래 타우 응집체의 시딩이 구조적 및 생리학적 수준에서 타우 병증을 매우 유사하게 모방하므로 이 모델이 타우 병증을 연구하는 데 유용한 도구가 될 수 있음을 시사합니다. 타우 시딩 연구를 시작하려면 지금 바로 문의하세요!
과학 뉴스
Protein Tag Labelling – Visualize the Invisible
October 29, 2025
전임상 생체 내 모델의 정기적인 재특성화를 통한 견고한 연구 결과 보장
September 23, 2025
블로그

혈관 질환과 치매의 연관성
October 21, 2025

저산소 공기가 파킨슨병 치료에 도움이 될 수 있습니다.
September 30, 2025
전문가들이 알츠하이머병 연구가 “티핑 포인트”에 있다고 말하는 이유
September 22, 2025

나노 플라스틱이 알츠하이머병을 가속화할까요?
September 16, 2025
회사 뉴스

Scantox, 지속 가능성 우수성 부문 EcoVadis 동메달 수상
July 28, 2025

Scantox 동물복지 및 과학적 무결성에 대한 당사의 약속을 강화하는 AAALAC 완전 인증 획득
June 27, 2025

2024 연례 보고서 발표
April 28, 2025

유전자 독성학 분야의 세계적 선도기업인 젠트로닉스(Gentronix)를 인수한 Scantox Group
September 9, 2024

