TDP-43 유도 루게릭병 마우스 모델
TAR DNA 결합 단백질(TARDBP 또는 TDP-43)은 점점 더 많은 신경 퇴행성 질환에서 중요한 역할을 하는 것으로 나타났습니다. 산발적 및 가족성 형태의 근위축성 측삭 경화증(ALS)과 밀접한 관련이 있지만, 신경 내 TDP-43 축적 및 응집은 전측두엽 변성(FTLD-TDP 또는 이전의 FTLD-U)과도 관련이 있습니다.
C57BL/6 마우스에서 루게릭병을 유도하기 위해 동물의 운동 피질에 인간 TDP-43을 발현하는 혈청형 9의 아데노-관련 바이러스(AAV) 입자(AAV9-GFP-hTDP-43)를 주입합니다. 대조군 동물에는 AAV9-GFP를 주입합니다. 생후 3개월에 유도하고 이후 6개월 동안 추적 관찰한 결과, AAV9-GFP-hTDP-43을 주입한 동물은 다음과 같이 나타났습니다:
- 초기 근력 약화
- 학습 결손
- 피질에서의 hTDP-43 발현
- 활성화된 미세아교세포 증가
- 유비쿼터스화 증가
- 뉴런 손실
AAV9-GFP-hTDP-43 주사 후 3개월이 지나면 이미 근육 약화가 관찰될 수 있습니다(그림 1).
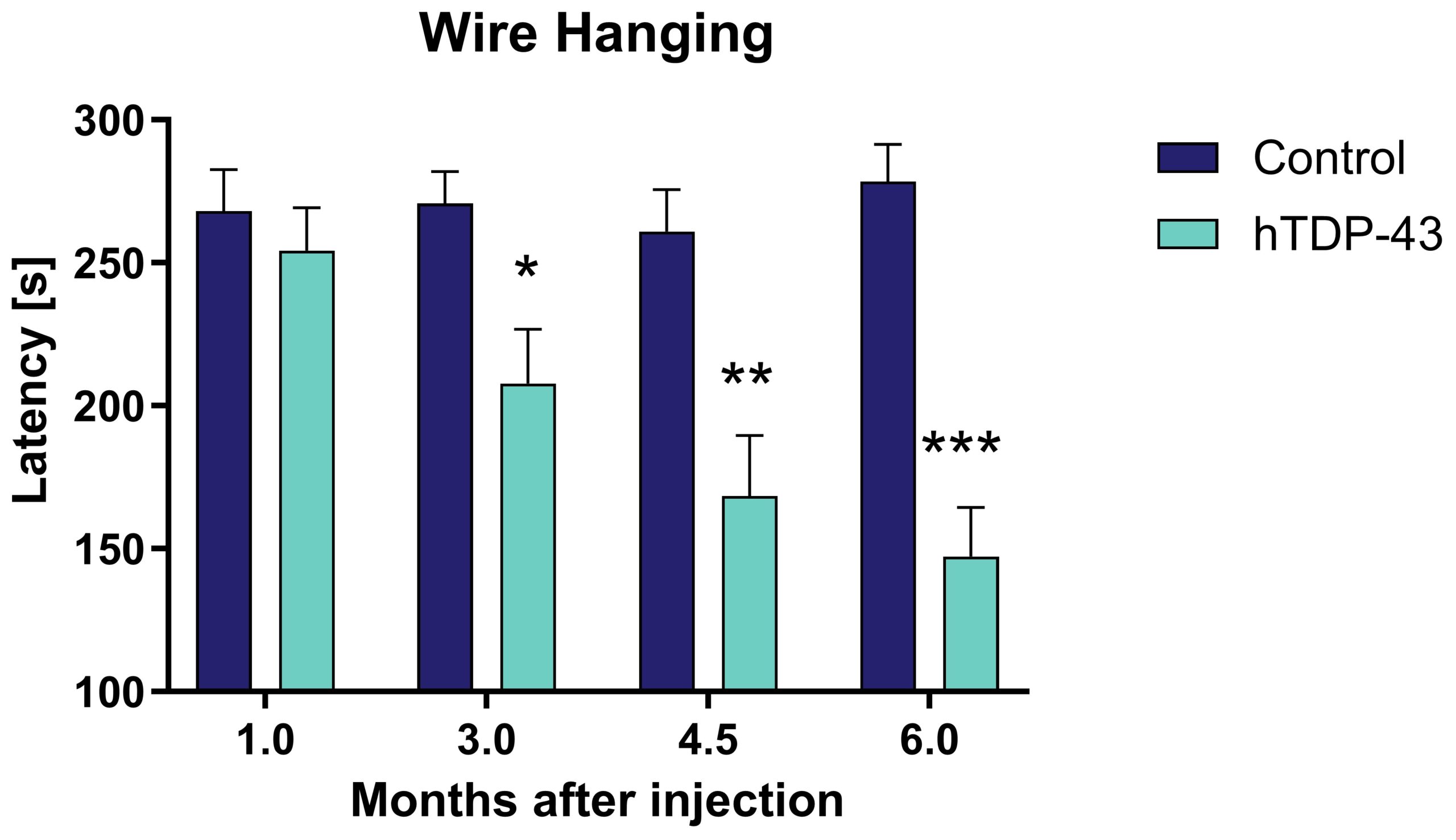
그림 1: AAV9-GFP-hTDP-43과 대조군 마우스에 와이어 매달기. 최대 300초까지 와이어에 매달리는 지연 시간을 측정했습니다. Bonferroni 사후 검정을 사용한 이원 분산 분석(Two-Way-ANOVA). 평균 + SEM. 대조군: n = 16, hTDP-43: n = 20. * p < 0.05, ** p < 0.01, *** p < 0.001.
AAV9-GFP-hTDP-43을 주입한 지 6개월 후, 생쥐는 피질에서 hTDP-43 단백질을 발현합니다(그림 2).
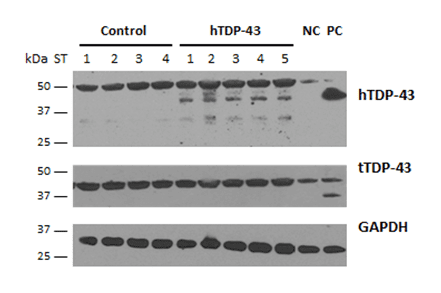
그림 2: 대조군 및 hTDP-43 마우스의 피질에서 인간 및 총 TDP-43의 발현. 주사 후 6개월이 지난 AAV9-GFP-hTDP-43 및 대조군 마우스의 피질 샘플을 RIPA 버퍼에서 균질화하고 GAPDH를 로딩 대조군으로 사용한 웨스턴 블롯 분석. PC: 양성 대조군 = 형질전환 TDP-43 마우스의 해마 RIPA 샘플. NC: 음성 대조군 = 처리되지 않은 야생형 마우스.
6개월 후 AAV9-GFP-hTDP-43을 주입한 마우스의 뇌에서 hTDP-43 발현과 활성화된 미세아교세포의 증가된 수준을 측정할 수 있습니다(그림 3).
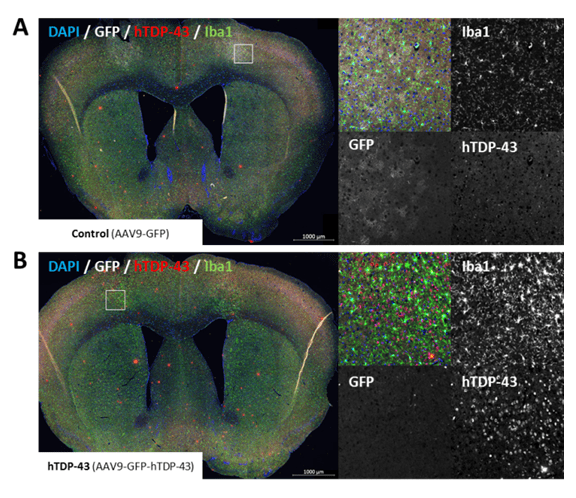
그림 3: 대조군 생쥐의 뇌에서 GFP(흰색), 인간 TDP-43(빨간색), Iba1(미세아교세포 마커, 녹색) 및 핵(DAPI, 파란색)의 면역 표지화 (A) 및 AAV9-GFP-hTDP-43 주입 모습 (B). 0.62mm로 관상적으로 절단된 뇌 샘플. 흰색 상자: 오른쪽에 확대된 주사 부위. 바이러스를 생후 3개월 생쥐의 운동 피질 영역 M1에 양측으로 주입했습니다. 샘플은 주사 후 6개월 후에 채취했습니다.
Scanox는 루게릭병 유발 모델에 대한 맞춤형 연구 설계를 제공하며, 고객의 특별한 관심사를 수용하기 위해 유연하게 대처합니다. 또한 연구 설계에 대한 조언과 제안도 기꺼이 해드립니다. 바이러스로 유도된 hTDP-43 마우스는 천천히 진행되는 루게릭병의 귀중한 모델입니다. 바이러스가 주입된 야생형 마우스는 적절한 연구 설계에 필요한 대조군 역할을 할 수 있습니다. 따라서 이 모델은 루게릭병에 대한 잠재적 치료의 효능을 평가하고 시간에 따른 치료 효과를 관찰하는 데 적합한 모델입니다.
루게릭병 동물 모델에서 귀사의 화합물의 효능을 평가해 드립니다! 가장 일반적인 판독 결과는 다음과 같습니다:
